文章摘要
研究人员开发出能修复血脑屏障并清除毒性蛋白的生物活性纳米颗粒,在小鼠实验中成功逆转阿尔茨海默病症状,为治疗该疾病提供了新思路。
文章总结
标题:新型纳米疗法清除β淀粉样蛋白 小鼠阿尔茨海默病症状逆转
研究人员开发出具有生物活性的纳米颗粒,能够修复大脑血脑屏障并清除毒性蛋白,成功逆转了小鼠的阿尔茨海默病症状,为治疗该疾病提供了新思路。
由西班牙加泰罗尼亚生物工程研究所(IBEC)与中国四川大学华西医院(WCHSU)联合领导的研究团队,与英国合作伙伴共同开发了一种新型纳米技术策略。与传统纳米药物不同,这种被称为"超分子药物"的纳米颗粒本身具有生物活性。
该疗法并非直接靶向神经元,而是专注于修复血脑屏障(BBB)——大脑抵御有害物质的天然防线。通过恢复血脑屏障功能,研究人员在动物模型中实现了阿尔茨海默病病理的逆转。
大脑血管系统的重要性
大脑是人体耗能最大的器官,占成人总能耗的20%,儿童则高达60%。约10亿条毛细血管构成的密集血管网络为神经元提供营养。在阿尔茨海默病中,血管功能减弱与疾病进展密切相关。
血脑屏障是大脑与血流间的保护屏障。研究团队通过靶向特定机制,成功清除了大脑产生的有害废物蛋白——在阿尔茨海默病中主要是β淀粉样蛋白(Aβ),其积累会破坏正常脑功能。
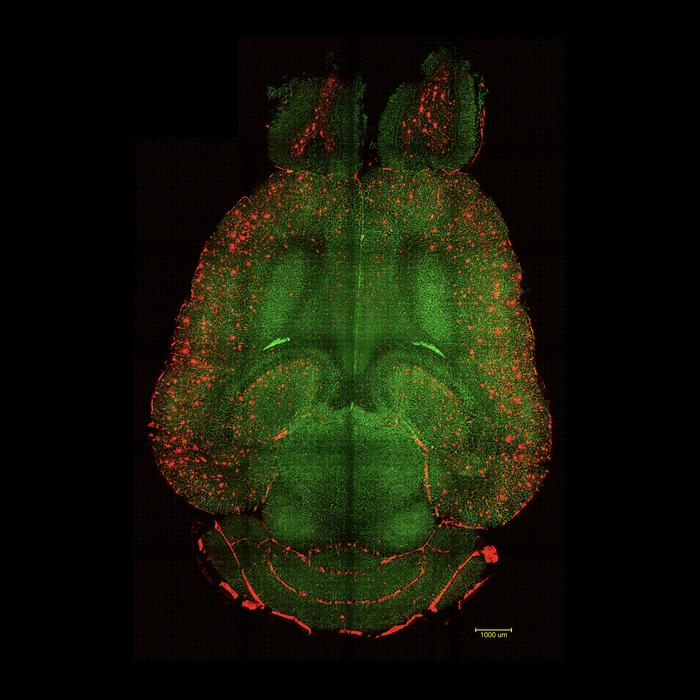 治疗前小鼠大脑:荧光显微镜显示Aβ斑块(红色)与血脑屏障血管(绿色)的积累情况。(图片来源:IBEC)
治疗前小鼠大脑:荧光显微镜显示Aβ斑块(红色)与血脑屏障血管(绿色)的积累情况。(图片来源:IBEC)
快速清除β淀粉样蛋白
在基因改造小鼠实验中,仅注射三剂超分子药物就显现显著疗效。研究第一作者陈俊阳表示:"注射1小时后,大脑内Aβ含量就减少了50-60%。"
行为测试显示,接受治疗的18月龄小鼠(相当于人类90岁)表现出与健康小鼠相当的行为能力。
恢复自然清除机制
研究负责人Giuseppe Battaglia教授解释:"纳米颗粒通过级联效应发挥作用——当血管功能恢复后,系统开始清除Aβ等有害分子,使整个系统重归平衡。"
正常情况下,LRP1蛋白负责转运Aβ通过血脑屏障排出。而超分子药物能模拟LRP1配体,重启清除机制,恢复血管功能。
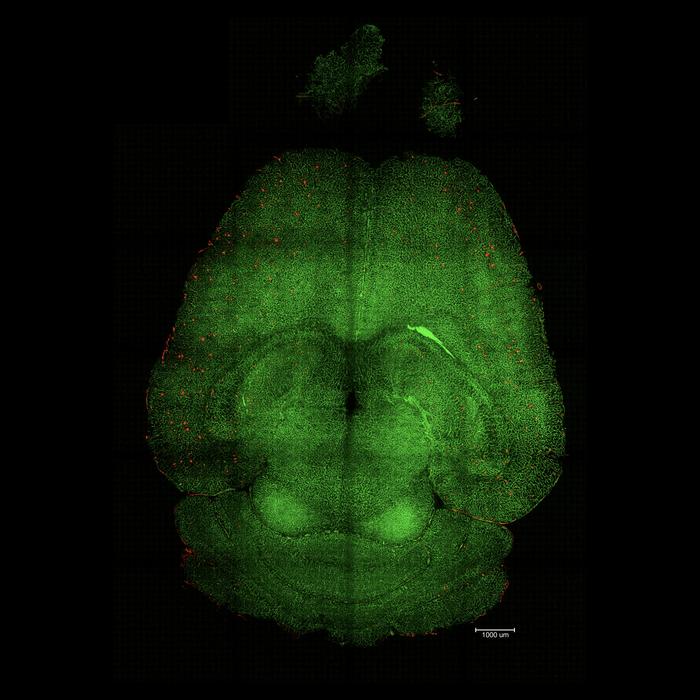 治疗后小鼠大脑:Aβ斑块显著减少。(图片来源:IBEC)
治疗后小鼠大脑:Aβ斑块显著减少。(图片来源:IBEC)
新型治疗可能性
研究人员采用自下而上的分子工程方法设计纳米颗粒,通过精确控制尺寸和表面配体实现高度特异性相互作用。IBEC研究员Lorena Ruiz Perez表示:"该研究在快速清除Aβ、恢复血脑屏障功能方面展现出卓越效果。"
这项研究证实,通过生物活性纳米颗粒恢复脑血管功能可以清除毒性蛋白并逆转认知衰退,为开发针对血管健康的神经退行性疾病疗法开辟了新途径。
评论总结
这篇评论围绕一项关于阿尔茨海默病(AD)小鼠模型的研究展开,主要观点可分为三类:
对淀粉样蛋白假说的质疑
- 多位评论者指出淀粉样蛋白假说缺乏可靠性,并提到相关研究可能存在学术不端(评论4:"Wasn't it revealed that the research supporting amyloid-beta plaque as the cause of Alzheimer's was fraudulent?")。
- 评论5强调小鼠模型与人类的差异:"billions of dollars in failed drug trials demonstrate that what works for those mice, doesn't work for humans"。
对研究价值的争议
- 批评者认为小鼠模型不适用于AD研究(评论2:"mouse models of Alzheimer's and/or ABeta simply not that useful";评论7直接质问"Why isn't 'in mice' an automatic flag for posting?")。
- 支持者如评论10则辩护称,动物模型是研究机制的宝贵工具:"Animal models are more accurately described as 'models of mechanism'"。
替代研究方向的建议
- 部分评论者提出应关注血脑屏障(BBB)修复(评论6:"this method focuses on repairing the blood-brain barrier")或淋巴系统功能(评论9:"Maybe the trick is going to be repairing the BBB and stimulating lymphatic function")。
- 评论8和评论11则分别从肠道微生物组和个体差异角度提出多元分析的必要性。
争议焦点在于:动物模型的可转化性、淀粉样蛋白假说的可信度,以及研究资源的分配合理性。支持者强调基础研究的机制价值(评论10),而反对者认为过度依赖小鼠模型浪费资源(评论5)。